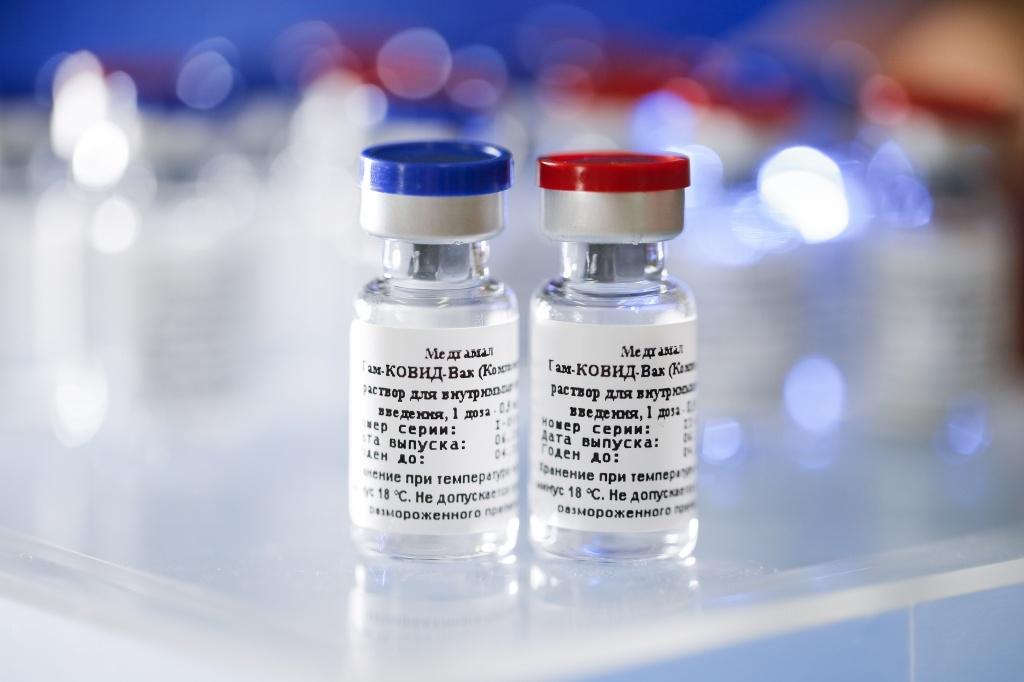
Ao comentar os atrasos no processo de aprovação da Sputnik V no Brasil, Fernando de Castro Marques, presidente da farmacêutica União Química, responsável pela vacina russa no país, disse nesta quarta-feira (3) que a empresa está "presa em um guia que a própria Anvisa (Agência Nacional de Vigilância Sanitária) tem condições de alterar, atualizar e modernizar".
A Sputnik V é produzida pelo Instituto Gamaleya e comercializada pelo Fundo de Investimento Direto da Rússia (RDIF). Atualmente é aplicada em nações como Rússia, Bielorrússia, Sérvia, Emirados Árabes, Argentina e Paraguai, além de ter sido aprovada pela OPAS (Organização Pan-Americana da Saúde).
Ontem (2), a revista científica The Lancet divulgou que o imunizante apresentou eficácia de 91,6% contra a covid-19. Hoje, o México foi mais um país a aprovar a aplicação da vacina.
"Depois da publicação da The Lancet, até a Angela Merkel entrou em contato interessada na Sputnik V para a Alemanha. Para se ter uma ideia, a revista não recebe um trabalho e publica. Ela audita. A fase 3 feita na Rússia foi auditada. Por isso o processo demora", disse Marques à Rádio Bandeirantes.
"Estamos presos em um guia que a própria Anvisa tem condições de alterar, atualizar ou modernizar. Temos produtos no Brasil com anticorpos monoclonais que estão sendo utilizados e não fizeram a fase 3 aqui. Acho que está tendo um rigor muito grande em um momento de pandemia. Não estamos nos furtando a fazer [os testes de fase 3], vamos fazer quando liberarem, mas entendemos que o governo tem segurança para autorizar a Sputnik V", completou.
O guia citado por ele é a publicação da Anvisa que estabelece os requisitos mínimos para solicitações de autorização de uso emergencial, em caráter experimental, de vacinas contra covid-19. Segundo a agência, o documento "tem como objetivo orientar as empresas desenvolvedoras de vacinas sobre os dados e as informações necessárias para apoiar a decisão na emissão de autorização temporária para vacinas experimentais".
O presidente da União Química adiantou que tem uma reunião agendada para a próxima sexta-feira (5) com equipes do Ministério da Saúde, especificamente do Programa Nacional de Imunizações (PNI).
"Espero que tenhamos um sinal positivo na negociação. Acredito que a Anvisa vai acabar liberando, baseada em tudo que está acontecendo no mundo", afirmou, ressaltando que, caso precise aguardar a conclusão dos testes de fase 3 no Brasil, a liberação da vacina teria um atraso de "no mínimo 60 ou 90 dias".
União Química fala em fornecer 150 milhões de doses
Na semana passada, Marques já havia informado ao blog que a companhia pretende fornecer 150 milhões de doses da Sputnik V ao país durante o ano de 2021, o que depende apenas de "interesse e aprovação".
"Entramos com pedido de uso emergencial na Agência Nacional de Vigilância Sanitária (Anvisa) para autorização de importação de 10 milhões de unidades já no primeiro trimestre. O fundo russo disponibilizou a quantia para embarque a curtíssimo prazo. Fizemos o pleito e estamos seguindo com o processo de registro definitivo na Anvisa, que, para isso, exige a fase 3 dos testes", disse.
"Estamos tratando do registro para produzir o IFA [o Ingrediente Farmacêutico Ativo] e não termos dependência externa. Estamos correndo com esse processo o quanto antes. O fundo russo dispõe, entre a produção deles e a nossa, o fornecimento de 150 milhões de unidades (durante o ano), se houver interesse e liberação no Brasil", completou.
MAIS INFORMAÇÕES AQUI:





